甲状腺癌是最常见的甲状腺恶性肿瘤。任何年龄均可发病,但以青壮年多见。 绝大多数甲状腺癌发生于一侧甲状腺腺叶,常为单个肿瘤。
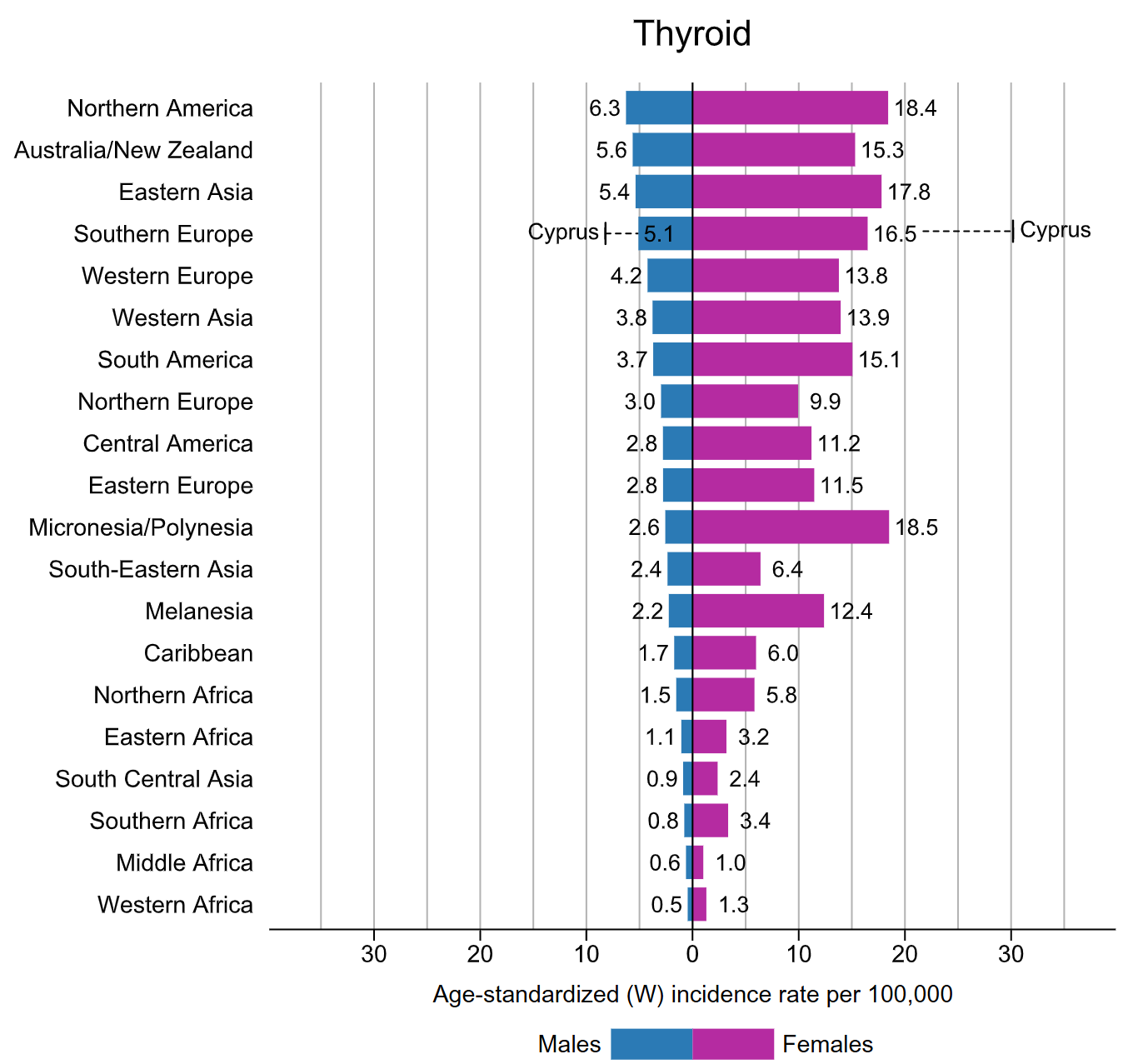
图1.2020年按性别划分的不同地区甲状腺癌发病率年龄标准化率。 比率按世界(W)年龄标准化男性比率的降序显示,并将男性和女性的最高国家比率叠加在一起。 资料来源:GLOBOCAN 2020 [1]。
世界卫生组织国际癌症研究机构(IARC)发布的数据显示,2020年, 全球甲状腺癌新发病例约为 58.6 万例,占所有癌症新发病例的 3.0%。同年, 全球白血病死亡病例约为 4.36 万例,占所有癌症新发病例的 0.4% [1]。 2022年,我国甲状腺癌新发病例达46.61万人,其中男性患者约为12.49万例, 女性患者约为34.12万例。同年,我国甲状腺癌死亡病例约为1.16万, 其中男性约为0.43万例,女性约为0.72万例 [2]。
甲状腺癌是一种起源于甲状腺滤泡上皮或滤泡旁细胞的恶性肿瘤,是最常见的内分泌系 统恶性肿瘤。在各种致病因素的作用下,甲状腺细胞发生基因突变等异常变化,导致细胞不受控制地增殖、分化异常,形成肿瘤组织,这些肿瘤细胞具有侵袭和转移的能力,可侵犯周围组织和器官,如气管、食管、喉返神经等,还可通过血液和淋巴系统转移到身体其他部位,如肺、骨、脑等,对患者的健康和生命造成严重威胁。
世界卫生组织(WHO 2022)将甲状腺癌分为以下主要类型:
1、分化型甲状腺癌(DTC)
起源于滤泡上皮细胞,保留部分甲状腺功能特征,占甲状腺癌的90%以上,预后较好。
(1) 乳头状甲状腺癌(Papillary Thyroid Carcinoma, PTC)
发病率:占甲状腺癌的85-90%,女性多见(男女比约1:3)。
病理特征:核呈毛玻璃样、核沟及核内假包涵体;常见砂粒体。
亚型:经典型、滤泡亚型、高细胞亚型、弥漫硬化型等。
BRAF V600E突变:约40-70%存在,与侵袭性相关。
(2) 滤泡状甲状腺癌(Follicular Thyroid Cancer, FTC)
发病率:占5-10%,与碘缺乏地区相关。
病理特征:滤泡结构为主,需通过包膜或血管侵犯确诊(与良性滤泡腺瘤鉴别)。
分子特征:RAS、PAX8/PPARγ融合基因常见。
2、髓样甲状腺癌(Medullary Thyroid Carcinoma, MTC)
起源:滤泡旁C细胞(神经内分泌来源),分泌降钙素。
发病率:占2-3%,部分为遗传性(25%)。
遗传相关性:
散发型(75%):无家族史,多为单侧。
家族型(25%):与多发性内分泌腺瘤病2型(MEN2)相关,由RET基因突变导致。
3、未分化甲状腺癌(Anaplastic Thyroid Cancer, ATC)
发病率:占1-2%,罕见但恶性度极高。
病理特征:细胞高度异型,失去甲状腺分化标志(如甲状腺球蛋白阴性)。
临床特点:多见于60岁以上,肿瘤迅速增大,压迫气管/食管(呼吸困难、吞咽困难)。常由分化型癌(如乳头状癌)转化而来。
4、其他罕见类型
甲状腺淋巴瘤:原发于甲状腺的B细胞淋巴瘤,多与桥本甲状腺炎相关。
鳞状细胞癌:极罕见,预后差。
甲状腺肉瘤:起源于间叶组织(如血管肉瘤)。
【甲状腺结节】
约90%的甲状腺癌以无痛性颈部肿块为首发症状。结节特征包括:质地硬(结节固定、边界不清,可能随吞咽活动度差),快速增大(尤其是未分化癌)。并非所有结节均为恶性(仅5-15%为癌),需结合超声、穿刺等评估。
【颈部淋巴结肿大】
乳头状癌易早期转移至颈部淋巴结(尤其颈侧区),可触及质硬、固定的肿大淋巴结。
【压迫症状】
呼吸困难:肿瘤压迫气管(如未分化癌迅速增大)。
吞咽困难:侵犯食管或周围组织。
声音嘶哑:侵犯喉返神经(单侧声带麻痹)。
Horner综合征:压迫颈交感神经链(眼睑下垂、瞳孔缩小等)。
【远处转移相关症状】
肺转移:咳嗽、咳血、呼吸困难(分化型癌常见)。
骨转移:骨痛、病理性骨折(滤泡状癌多见)。
脑转移:头痛、癫痫、神经功能障碍(罕见)。
【激素相关症状(仅特定类型)】
髓样癌:分泌降钙素或5-羟色胺,可致腹泻、面部潮红(类癌综合征)。
未分化癌:可能因肿瘤坏死释放炎性因子,导致发热、体重下降。
【局部并发症】
气道梗阻:肿瘤压迫气管导致窒息(未分化癌风险最高)。
喉返神经损伤:手术或肿瘤侵犯致永久性声音嘶哑。
甲状旁腺功能减退:手术误切甲状旁腺导致低钙血症(手足抽搐、肌肉痉挛)。
【全身并发症】
远处转移相关器官衰竭:如肺转移致呼吸衰竭,肝转移致肝功能衰竭。
恶病质:晚期患者出现极度消瘦、贫血、乏力。
【治疗相关并发症】
放射性碘治疗:唾液腺炎、骨髓抑制、继发肿瘤(罕见)。
靶向治疗(如索拉非尼):高血压、手足综合征、蛋白尿。
甲状腺癌的诊断和检测方法多样,主要包括体格检查、影像学检查、实验室检查、细针穿刺活检以及分子检测等。
1、影像学检查
影像学检查是甲状腺癌诊断的重要手段,主要包括以下几种:
超声检查:超声检查利用高频声波显示甲状腺的形态和结构,能够发现微小的异常肿块和结节。 超声检查具有无创、无痛、无辐射等优点,是甲状腺癌筛查的首选影像学检查方法。
CT和MRI:CT和MRI可用于评估甲状腺癌原发病灶、颈淋巴结的病变范围及与周围重要器官的关系。
2、实验室检查
实验室检查包括甲状腺功能检测、甲状腺自身抗体检测和肿瘤标志物检测:
甲状腺功能检测:包括甲状腺素(T4)、三碘甲状腺原氨酸(T3)、游离T4(FT4)、游离T3(FT3)以及促甲状腺激素(TSH)的测定。
甲状腺自身抗体检测:包括抗甲状腺球蛋白抗体(TgAb)和甲状腺过氧化物酶抗体(TPOAb)。
肿瘤标志物检测:血清甲状腺球蛋白(Tg)和降钙素(Ctn)是重要的肿瘤标志物,尤其在怀疑髓样癌(MTC)时,应同时检测癌胚抗原(CEA)。
3、细针穿刺活检(FNAB)
超声引导下的细针穿刺活检是术前评估甲状腺结节良恶性的敏感度和特异度最佳方法。 FNAB洗脱液中的Tg和Ctn水平检测可辅助诊断分化型甲状腺癌(DTC)和转移淋巴结。
4、分子检测
对于经FNAB仍不能确定良恶性的甲状腺结节,可进行分子检测,包括:
BRAF突变:BRAF V600E突变在甲状腺乳头状癌中检出率较高,检测到该突变几乎可以预测恶性。
RET/PTC重排:与多种融合伴侣融合,常见于儿童实性梁状型PTC和弥漫硬化型PTC。
RAS突变:在滤泡状癌和部分乳头状癌中常见,但其诊断价值低于BRAF突变。
其他分子标志物:如PAX8/PPARγ重排、PIK3CA突变、TP53突变等。
5、人工智能
人工智能技术在甲状腺癌的诊断中也逐渐得到应用,通过分析影像学和病理学数据,提高诊断的准确性和效率。
甲状腺癌的病因尚未完全明确,但研究表明可能与以下多种因素相关:
(一)电离辐射暴露
儿童期辐射暴露:儿童时期(尤其是青春期前)的颈部或头颈部接受电离辐射(如X线、核辐射等)是明确的危险因素。辐射可能直接损伤甲状腺细胞的DNA,导致基因突变。
核事故或医疗辐射:核泄漏事件(如切尔诺贝利事故)中暴露于放射性碘(如碘-131)的人群,甲状腺癌发病率显著升高。
(二)遗传因素
家族性甲状腺癌:约5%-10%的甲状腺癌具有家族遗传倾向,可能与基因突变(如RET、BRAF、RAS等)相关。
遗传综合征:多发性内分泌腺瘤病2型(MEN2):与RET基因突变相关,显著增加甲状腺髓样癌风险。
家族性甲状腺非髓样癌:如Cowden综合征(PTEN基因突变)、APC基因相关息肉病等。
(三)激素水平影响
雌激素作用:女性发病率约为男性的3倍,可能与雌激素促进甲状腺细胞增殖有关。妊娠、口服避孕药等雌激素水平升高的状态可能增加风险。
促甲状腺激素(TSH):长期TSH水平升高(如甲状腺功能减退未控制)可能刺激甲状腺细胞异常增生。
(四)碘摄入异常
碘缺乏:长期碘缺乏可导致甲状腺代偿性增生(如地方性甲状腺肿),可能增加滤泡状癌风险。
碘过量:过量碘摄入可能与乳头状癌风险升高相关,但具体机制仍需进一步研究。
(五)环境与生活方式
化学物质暴露:长期接触某些化学物质(如多氯联苯、硝酸盐、重金属等)可能干扰甲状腺功能。
肥胖:肥胖者体内脂肪因子(如瘦素、炎症因子)可能促进甲状腺癌发生。
吸烟与饮酒:部分研究显示吸烟可能与甲状腺癌风险降低相关(争议性结论),而酒精的作用尚不明确。
(六)慢性炎症与免疫因素
桥本状腺炎:慢性淋巴细胞性甲状腺炎(桥本病)患者中,甲状腺乳头状癌的发生率略高于普通人群,可能与长期炎症刺激有关。
免疫失调:自身免疫性疾病(如Graves病)患者中甲状腺癌风险可能升高。
甲状腺癌的分子生物学致病机制是一个多因素、多步骤的复杂过程,涉及遗传突变、表观遗传调控异常、信号通路失调及微环境重塑等关键环节。
1、关键信号通路异常
【MAPK/ERK通路】
BRAF V600E突变:约60%的甲状腺乳头状癌(PTC)中存在BRAF基因突变(尤其是V600E),导致MAPK通路持续激活,促进细胞增殖和侵袭。该突变与肿瘤的侵袭性及放射性碘治疗抵抗密切相关。
RAS基因突变:在滤泡状癌(FTC)和Hurthle细胞癌中常见(HRAS、NRAS、KRAS突变),通过激活MAPK和PI3K-AKT双通路驱动肿瘤发生。
RET/PTC重排:约20%的PTC中存在RET基因与其他基因(如CCDC6、NCOA4)的融合,形成RET/PTC癌基因,模拟受体酪氨酸激酶的持续激活,多见于辐射暴露(如切尔诺贝利核事故相关病例)。
【PI3K-AKT-mTOR通路】
PIK3CA突变及PTEN缺失:常见于滤泡状癌和未分化癌(ATC),通过PI3K-AKT通路促进细胞存活和代谢重编程,与肿瘤去分化相关。
mTOR激活:在PTC中,mTORC2复合物的激活通过磷酸化AKT Ser473促进转移和治疗抵抗。
2、关键基因突变与分子分型
TP53突变:在未分化癌(ATC)中突变率高达70-80%,导致基因组不稳定性和细胞周期失控。
TERT启动子突变:与肿瘤进展和不良预后相关,通过端粒酶活性增强赋予癌细胞无限增殖能力。
EIF1AX突变:在低分化癌(PDTC)和未分化癌中常见,影响翻译起始复合物的功能,可能通过蛋白质合成失调促进恶性转化。
SWI/SNF复合物基因突变:如ARID1A,参与染色质重塑,突变导致表观遗传调控异常。
3、表观遗传学改变
DNA甲基化异常:抑癌基因(如RASSF1A)启动子高甲基化导致沉默,而促癌基因(如HOXA10)低甲基化激活。
非编码RNA调控:
miRNA:如miR-21过表达抑制PTEN,促进PI3K-AKT通路激活;miR-200家族调控上皮-间质转化(EMT)。
lncRNA:HOTAIR通过结合PRC2复合体沉默抑癌基因,增强侵袭性。
4、激素与受体互作机制
TSH-TSHR信号:促甲状腺激素(TSH)通过结合TSH受体(TSHR)激活cAMP通路,长期高TSH刺激(如碘缺乏或辐射后)可促进甲状腺细胞增殖及癌变。
自身免疫性抗体:在Graves病中,激活型抗体(如M22)通过“推”(push)机制激活TSHR,导致甲状腺激素过度分泌;而桥本甲状腺炎中抑制型抗体(如K1-70)竞争性阻断TSH结合,引发甲减。
5、肿瘤微环境与代谢重编程
免疫逃逸:肿瘤相关巨噬细胞(TAM)分泌IL-10、TGF-β抑制抗肿瘤免疫;PD-1/PD-L1轴在部分亚型(如髓样癌)中参与免疫抑制。
代谢异常:
Warburg效应:癌细胞依赖有氧糖酵解,GLUT1和HK2表达上调支持快速增殖。
脂代谢异常:脂肪酸合成酶(FASN)过表达提供膜合成原料,并生成信号分子(如棕榈酸酯)促进生长。
甲状腺癌的西医治疗需根据病理类型、分期、分子特征及患者个体情况制定方案。
(一)手术治疗
手术是大多数甲状腺癌的首选治疗,关键目标是彻底切除肿瘤并降低复发风险。
1、手术方式选择
【甲状腺全切术】
适应症:肿瘤直径>1cm、多灶癌、甲状腺外侵犯、淋巴结转移、家族史或辐射暴露史。
优势:便于术后放射性碘治疗及监测甲状腺球蛋白(Tg)。
【甲状腺叶切除术】
适应症:单发微小癌(≤1cm)、无高危因素(如家族史、辐射史)、局限于一叶且无淋巴结转移。
2、淋巴结清扫
中央区清扫(VI区):所有分化型癌(尤其T3-T4期)推荐预防性清扫。
侧颈清扫(II-V区):临床或影像学提示淋巴结转移时进行。
注意:术中需保护喉返神经及甲状旁腺,术后可能出现声音嘶哑或低钙血症(需补钙及维生素D)。
(二)放射性碘治疗(RAI)
主要用于分化型甲状腺癌(乳头状癌、滤泡状癌)术后清除残留甲状腺组织或转移灶。
1、治疗指征
高危患者:甲状腺外侵犯、淋巴结转移>3cm、远处转移。
中危患者:酌情选择(如肿瘤1-4cm伴血管侵犯)。
低危患者:通常不推荐(微小癌且无转移)。
2、剂量选择
清除残留甲状腺:30-100mCi(低剂量方案减少唾液腺损伤)。
治疗转移灶:100-200mCi,需根据病灶摄碘能力调整。
副作用:唾液腺炎(含维生素C或酸味食物促唾液分泌)、暂时性骨髓抑制。
(三)TSH抑制治疗
通过左甲状腺素(LT4)将TSH控制在目标范围,抑制肿瘤生长。
TSH目标值
高危复发:TSH<0.1 mU/L(需平衡骨质疏松及心律失常风险)。
中危:TSH 0.1-0.5 mU/L。
低危:TSH 0.5-2.0 mU/L。
监测:每3-6个月检测FT4、TSH,调整剂量。
(四)靶向与免疫治疗
针对晚期或难治性甲状腺癌(如未分化癌、碘难治性分化型癌)。
靶向药物
多激酶抑制剂:
仑伐替尼:用于RAI难治性分化型癌,延长无进展生存期(PFS)。
凡德他尼/卡博替尼:用于髓样癌,抑制RET及VEGFR。
BRAF抑制剂:达拉非尼+曲美替尼:BRAF V600E突变未分化癌的一线方案。
免疫治疗 PD-1/PD-L1抑制剂:用于未分化癌或高突变负荷肿瘤(如帕博利珠单抗)。
(五)放射治疗(EBRT)
主要用于无法手术的局部进展或复发灶,或骨/脑转移的姑息治疗。
调强放疗(IMRT):精准靶向病灶,减少周围组织损伤。
适应症:未分化癌、髓样癌术后残留、疼痛性骨转移。
(六)化疗
适应症:未分化癌或晚期其他类型癌的联合治疗。
方案:多柔比星+铂类,但疗效有限(缓解率<30%)。
(七)个体化治疗策略
分化型癌(PTC/FTC):手术+RAI+TSH抑制为主,晚期联用靶向药。
髓样癌(MTC):手术扫,RET突变者用凡德他尼。
未分化癌(ATC):手术(若可切除)→放疗+化疗+靶向/免疫治疗(BRAF/MEK抑制剂)。
碘难治性癌:仑伐替尼或索拉非尼控制进展。
本病相当于中医病名石瘿范畴,中医认为其主要病因病机为情志抑郁,肝气郁滞, 脾失健运,痰湿内生,气、血、痰相互凝结而成。
【辨证用方】
甲状腺癌的辨证,当辨明虚、实。以颈前肿块,伴面部热、心烦易怒为主症者, 多为实证;以颈前肿块伴心悸气短乏力神疲为主症者,多为虚证。证属实者, 治以清肝泻火,软坚散结;证属虚者,治以养心益肾,化痰散结。
1.肝火旺盛证
【主症】颈前肿块,灼热疼痛,咳唾黄痰,声音嘶哑,面部烘热,口干口苦, 小便黄赤,舌红苔黄,脉细数。
【治法】清肝泻火,软坚散结。
【主方】栀子清肝合藻药汤(潘敏求经验方)
【组成与用法】栀子10g,丹皮10g,柴胡10g,赤芍12g,当归10g,海藻10g, 黄药子10g,瓜蒌15g,土贝母12g,丹参10g,夏枯草15g,生牡蛎(先煎)30g。 水煎服。
【功能主治】清泻肝火,软坚散结。主治甲状腺癌肝火旺盛证。
【加减应用】肋胁胀痛者,加香附、郁金; 腹胀,大便秘结者,加枳壳、 大黄(后下);口干咽燥,加麦冬、沙参。
2.痰毒内蕴证
【主症】颈前肿块,胀痛,咳嗽痰多,胸闷纳差,大便干舌质暗红,舌厚腻,脉数滑。
【治法】化痰软坚,解毒散结。
【主方】海藻玉壶汤加味方(《中华肿瘤治疗大成》)
【组成与用法】海藻10g,昆布10g,陈皮10g,法夏10g,贝母10g,连翘15g, 当归10g,川芎10g,茯苓12g,香附10g,郁金15g,穿山甲(先煎)15g, 土贝母12g,蚤休15g,石见穿15g,天南星10g。水煎服。
【功能主治】理气消瘿,化痰散结。主治甲状腺癌痰毒内蕴证。
【加减应用】郁久化火、灼热、舌红者,加丹皮、栀子、夏枯草;神疲乏力,便溏者, 加白术、山药。
3.气滞血瘀证
【主症】颈前肿胀,质硬固定,胸闷气憋,心烦易怒,头痛目眩,舌质紫暗, 苔薄白,脉弦涩。
【治法】疏肝行气,祛瘀散结。
【主方】柴胡疏肝散加减方(《中华肿瘤治疗大成》)
【组成与用法】柴胡10g,陈皮10g,重楼10g,枳壳10g,赤芍10g,丹参15g, 炮穿山甲(先煎)12g,莪术10g,栀子10g,夏枯草10g,龙葵20g,郁金10g, 生牡蛎(先煎)30g,海藻12g,制整甲(先煎)12g,猫爪草15g。水煎服。
【功能主治】疏肝解郁,活血散结。主治甲状腺癌气滞血瘀证。
【加减应用】神疲乏力、大便溏薄者,加茯苓、白术;纳呆脘痞者,加藿香、惹苡仁、鸡内金。
4.心肾阴虚证
【主症】颈部肿块,绵绵不息,心悸气短,全身乏力,自汗盗汗,精神萎靡, 头晕目眩,腰膝酸软,舌质暗红,苔黄,脉沉细。
【治法】养心益肾,化痰散结。
【主方】生脉散合二至丸加减方(《中华肿瘤治疗大成》)
【组成与用法】党参15g,麦冬10g,五味子10g,黄精15g,黄芪20g,女贞子20g, 旱莲草10g,煅牡蛎(先煎)15g,仙鹤草10g,海藻10g,黄药子10g,山慈菇15g。 水煎服。
【功能主治】益气生津,敛阴止汗。主治甲状腺癌心肾阴虚证。
【加减应用】口干口渴、苔少者,加玉竹、芦根; 纳差便溏者,加茯苓、白术。
甲状腺癌的总体预后较好,尤其是分化型甲状腺癌(如乳头状癌和滤泡状癌)。根据计数据,甲状腺癌患者的5年生存率可达98%,10年生存率约为90%,部分类型如乳头状癌甚至可达99%以上。
甲状腺癌的预防与护理需结合其已知危险因素及患者的具体情况,通过规避风险、早期筛查、科学治疗及生活管理降低发病风险并改善预后。
1、减少电离辐射暴露
儿童及青少年:避免不必要的头颈部CT、X线检查(除非临床必需)。
职业防护:核工业、放射科工作人员需严格穿戴防护设备。
核事故应对:接触放射性碘后,及时服用碘化钾(KI)阻断甲状腺吸收。
2、遗传筛查与干预
RET基因突变家族(MEN2):建议儿童期行预防性甲状腺切除术。
家族性非髓样癌(FNMTC):定期甲状腺超声筛查(每年1次)。
基因检测:对有甲状腺癌家族史者,可检测BRAF、RAS、TERT等基因突变。
3、控制体重与代谢综合征
目标BMI:保持18.5-24.9 kg/m²,肥胖者(BMI≥30)减重5-10%。
饮食建议:低糖、低脂、高纤维,减少加工食品摄入。
运动习惯:每周≥150分钟中等强度运动(如快走、游泳)。
4、合理碘摄入
普通人群:通过碘盐(每日5-6g)及海产品(每周1-2次)维持适量碘营养。
高碘地区(如沿海):减少海带、紫菜等高碘食物。
低碘地区(如内陆):优先选择加碘盐,定期监测尿碘。
5、减少环境毒素接触
内分泌干扰物:避免使用含双酚A(BPA)的塑料容器(如矿泉水瓶、外卖盒)。选择无邻苯二甲酸盐的化妆品、儿童玩具。
重金属:减少接触工业污染区,食用重金属检测合格的海产品。
6、戒烟限酒
吸烟:虽可能降低甲状腺癌风险,但增加肺癌等疾病风险,建议戒烟。
酒精:男性≤25g/日,女性≤15g/日 (如啤酒≤500ml/日)。
1、术后护理
伤口护理:术后1周内保持颈部清洁干燥,避免感染。观察有无红肿、渗液,及时就医处理。
甲状旁腺功能保护:术后监测血钙,若出现手足麻木、抽搐,立即补充钙剂与活性维生素D。
嗓音康复:喉返神经损伤者,可进行嗓音训练或声带填充术。
2、生活方式调整
饮食管理:放射性碘治疗期间:低碘饮食(避免海产品、碘盐)2-4周,提升¹³¹I疗效。
长期饮食:均衡摄入蛋白质、维生素,避免过量十字花科蔬菜(如卷心菜、西兰花可能抑制碘吸收)。
运动建议:术后2-4周开始轻度活动(如散步),逐步恢复至正常运动强度。
心理支持:加入患者互助团体,必要时寻求心理咨询,缓解焦虑或抑郁情绪。
3、长期用药管理
左甲状腺素(LT4):每日空腹服用,与钙剂、铁剂间隔4小时以上。定期检测TSH,调整剂量(分化型癌需TSH抑制治疗)。
靶向药物(如仑伐替尼):监测血压、尿蛋白,及时处理手足综合征(保湿、避免摩擦)。
4、定期随访与监测
【分化型癌(DTC)】
超声:术后第1年每6个月1次,此后每年1次。
甲状腺球蛋白(Tg):术后每6个月检测(TSH刺激后更敏感)。
【髓样癌(MTC)】
降钙素/CEA:每3-6个月检测,倍增时间<6个月提示进展。
影像学:颈部MRI/CT每年1次,怀疑转移时行PET-CT。
【未分化癌(ATC)】
每1-2个月复查CT评估疗效,及时调整治疗方案。
1、高蛋白摄入
2、补充充足的维生素和矿物质
3、适量的脂肪
4、少食多餐
5、选择易消化的食物
6、控制碘的摄入
1、避免高脂肪类食物
2、避免高糖类食物
3、避免海鲜类食物
4、避免辛辣刺激性食物
5、避免油炸、腌制食物
6、避免咖啡等兴奋性饮料
7、戒烟限酒
食疗方 1
【组成】南瓜55克,虾皮20克,大白菜适量,面粉适量,葱姜、蒜、油各适量。
【制作】面粉加水调成硬度适中的面粉糊;将南瓜、大白菜虾皮、葱、姜、蒜一起剁碎制成馅,入一勺面糊摊成饼状,加一匙面糊摊匀,馅上再摊一层面粉糊,人油锅炸熟即可。
【功效】 适用于饮食不振、浮肿、少尿的癌症病人。
备注:更多食疗方见肿瘤药膳专栏,或点击本页相关文章栏目相应文章链接阅读。