胰腺癌可谓是知名度最高的癌症类型之一,包括原苹果公司CEO史蒂夫·乔布斯、 世界知名男高音歌手帕瓦罗蒂在内的多位名人均因罹患胰腺癌而不治离世 [1]。 胰腺癌是一种恶性程度极高的消化系统肿瘤,由于其位置隐匿、早期症状不典型, 多数患者在确诊时已处于晚期,治疗效果往往不佳,预后较差,因此被称为 “癌中之王”。近年来,随着生活方式的改变、人口老龄化等因素的影响, 胰腺癌的发病率呈逐渐上升趋势,给社会和家庭带来了沉重的负担。对胰腺癌的 研究和防治已成为全球医学界关注的重点领域,涉及病因学、早期诊断技术、 治疗方法创新等多个方面,旨在提高胰腺癌患者的生存率和生活质量。
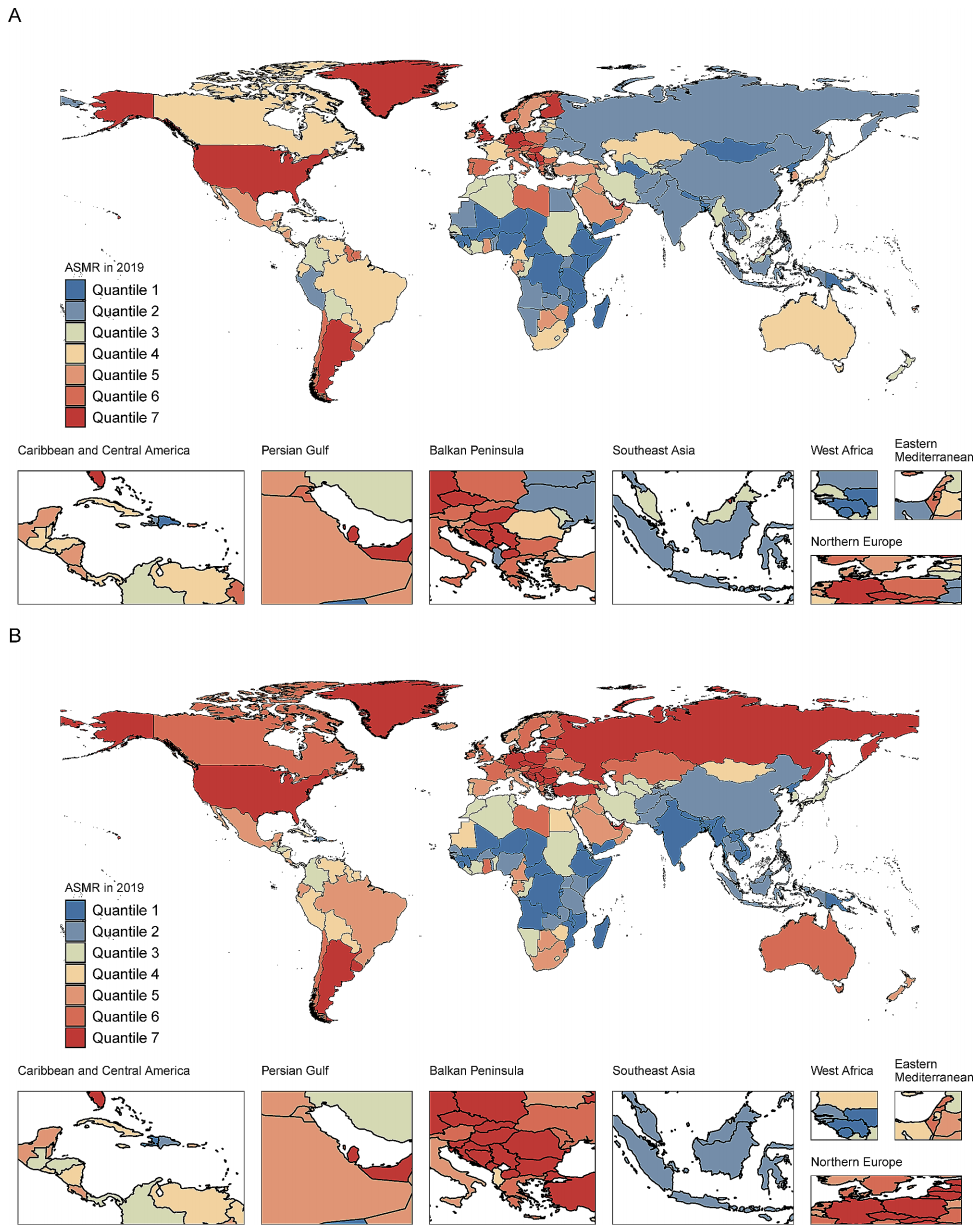
图1.2019年所有国家/地区因(A)高空腹血糖和(B)高身体质量指数导致的 年龄标准化胰腺癌死亡率。ASMR:年龄标准化死亡率 [3]。
根据国际癌症研究机构 (IARC)发布的全球癌症数据,胰腺癌在全球范围内的发病率 呈上升趋势。在 2020 年,全球胰腺癌新发病例约 49.6 万例,死亡病例约 46.6 万例 [2]。胰腺癌的发病率在不同地区存在差异。欧美国家发病率相对较高,如美国、 加拿大、北欧等地区 [3]。在非洲、亚洲的一些发展中国家发病率相对较低,但近年来 也有明显上升趋势。
在中国,随着经济的发展和生活方式的改变,胰腺癌的发病率也在不断上升。2020 年 中国胰腺癌新增病例为11.87万例,其中男性为6.71万例,女性为5.15万例。同年, 中国胰腺癌死亡病例10.63万例,其中男性为6.11万例,女性为4.52万例 [4]。
胰腺癌是指原发性胰腺导管腺癌,它占所有胰腺肿瘤的90%以上。胰腺癌是一种高度恶性的肿瘤,发病隐匿,进展迅速,治疗效果及预后极差,被称为“癌中之王”。主要起源于胰腺上皮细胞,具有“四高”和“五低”的特点:
四高:高发病率、高死亡率、高复发转移率、高手术风险。
五低:低早期诊断率、低切除率、低药物有效率、低5年生存率、低生活质量。
胰腺癌的分类方法多样,主要包括按发病部位、组织学类型和临床分期进行分类。
【按发病部位分类】
胰头癌:占胰腺癌总发病率的60%-70%,常压迫和浸润导致胰管管腔狭窄或闭塞,远端易继发胰腺炎,患者会出现腹痛、梗阻性黄疸等症状。
胰体癌:占胰腺癌总发病率的20%-30%,患者常出现食欲缺乏、上腹饱胀、消化不良、便秘或腹泻,伴随消瘦、体重减轻等。
胰尾癌:占胰腺癌总发病率的5%-10%,患者常出现食欲缺乏、上腹饱胀、消化不良、便秘或腹泻,伴随消瘦、体重减轻等。
全胰癌:约占胰腺癌总发病率的5%,可由胰头、胰体、胰尾的癌症进一步发展导致。
【按组织学类型分类】
导管腺癌:占胰腺癌的80%-90%,主要由分化不同程度的导管样结构的腺体构成,伴有丰富的纤维间质。
特殊类型的导管起源的癌:
多形性癌:亦称巨细胞癌,可能为导管癌的一种亚型。由奇形怪状的单核或多核瘤巨细胞,甚至梭形细胞构成,有时可类似破骨细胞的巨细胞或绒癌样细胞。
腺鳞癌:偶见于胰腺,可能为胰管上皮鳞化恶变的结果。肿瘤由腺癌和鳞癌成分组成。纯粹的鳞癌在胰腺相当罕见。
粘液癌:切面可呈胶冻状,极相似于结肠的胶样癌。光镜下,肿瘤含有大量粘液,形成粘液池。细胞可悬浮其中或散在于粘液池的边缘。
粘液表皮样癌和印戒细胞癌:在胰腺中偶可见到。
纤毛细胞癌:形态与一般导管癌相同,其特点是有些细胞有纤毛。
腺泡细胞癌:仅占1%,肿瘤细胞呈多角形、圆形或矮柱形。核圆、常位于基底部。瘤细胞排成腺泡状或条索状,胞浆强嗜酸性颗粒状。电镜和免疫组织化学均显示瘤细胞的腺泡细胞特征,如丰富的粗面内质网和酶原颗粒。
小腺体癌:为少见类型的胰腺癌。胰头部较为多见。镜下,肿瘤由很多小腺体结构及实性癌巢组成,其间有纤细的纤维间隔。细胞可为立方或柱状,核较为一致,常见小灶性坏死,在小腺体的腔缘可见少量粘液。
大嗜酸性颗粒细胞性癌:此型肿瘤罕见,其肿瘤细胞具有丰富的嗜酸性颗粒性胞浆,核圆形或卵圆形,排列成小巢状。其间有纤维间隔分隔。电镜瘤细胞胞浆内充满肥大的线粒体。
小细胞癌:胰腺的小细胞癌形态上与肺小细胞癌相似,约占胰腺癌的1%-3%。由一致的小圆细胞或燕麦样细胞构成,胞浆很少,核分裂很多,常有出血坏死,NSE免疫组化染色阳性,此型预后很差。
【按临床分期分类】
Ⅰ期:T1 N0 M0;T1 Nx M0;Tx N0 M0;Tx Nx M0。
Ⅱ期:T2 N0 M0;T2 Nx M0;T3 N0 M0;T3 Nx M0。
Ⅲ期:任何T,N1,M0。
Ⅳ期:任何T,任何N,M1。
上腹部压痛:上腹部压痛是胰腺癌早期唯一体征。随着肿瘤的发生,影响内脏被膜所致的牵拉反应,会使疼痛日渐加重。
肝肿大:50%-70%的患者可有肝脏肿大,其原因以淤胆为主,偶为门静脉高压或癌肿转移所致。
胆囊肿大:胰腺癌出现肝外阻塞性黄疸时,有时可扪及肿大胆囊。按照Courvoisier法则(无痛性黄疸一胆囊增大),与胆石症作鉴别诊断具有重要意义。
腹部肿块:胰腺位置深,胰腺癌患者一般不易触到腹部肿块。一旦扪及肿块,不论原发灶或转移灶多表明病程已属晚期。
腹部血管杂音:胰腺癌压迫肠系膜上动脉、腹主动脉或脾动脉时,腹部可出现吹风样血管杂音。
腹水征:胰腺癌晚期因腹膜转移、门静脉血栓形成或癌肿压迫门静脉,可有腹水征表现。
血栓性静脉炎:胰腺癌患者可出现游走性血栓性静脉炎或小腿深部静脉血栓形成。
淋巴结肿大:晚期胰腺癌患者可在颈部、腋下等处扪及肿大的淋巴结。
食欲不振:随着胰腺癌的进展,胰腺功能异常,影响胆汁分泌,导致消化能力降低,从而出现食欲不振的症状。
腹胀:胰腺的外分泌功能有助于促进食物的消化,胰腺出现肿瘤会导致消化能力变差,甚至引发腹胀症状。对于药物可缓解,但呈现进行性加重趋势的腹胀,最好提高警惕。
消瘦和乏力:80%~90%的胰腺癌患者在疾病初期即有消瘦、乏力、体重减轻,与缺乏食欲、焦虑和肿瘤消耗等有关。
消化道症状:当肿瘤阻塞胆总管下端和胰腺导管时,胆汁和胰液体不能进入十二指肠,常出现消化不良症状。胰腺外分泌功能损害可能导致腹泻。晚期胰腺癌侵及十二指肠,可导致消化道梗阻或出血。
黄疸:与胆道出口梗阻有关,是胰头癌最主要的临床表现,可伴有皮肤瘙痒、深茶色尿和陶土样便。
持续的腹部或背部疼痛:腹痛和背痛是胰腺癌患者常见的症状,但它们往往不易被察觉。早期可能只是轻微的不适,许多人会忽视,认为是消化不良。
皮肤或眼白发黄的迹象:黄疸是胰腺癌的一个显著症状,通常由肿瘤压迫胆道,妨碍胆汁排泄而引起。当身体出现皮肤或眼白发黄,尿液变深及粪便变淡时,通常意味着病情已经进入了较为严重的阶段。
频繁的消化不良与恶心呕吐:消化不良、恶心和呕吐是另一组与胰腺癌相关的症状。这是由于肿瘤对胰腺的压迫,导致其监测消化酶的正常分泌受到影响,进而诱发胃肠道的不适。
胆道梗阻:胰腺癌最常见的并发症,临床上一般通过经皮胆道引流或者胆总管空肠吻合术来处理胆道梗阻症状。
十二指肠梗阻:是导致胰腺癌患者死亡的一个重要因素,治疗十二指肠梗阻的情况可以通过胃空肠吻合术来加强营养治疗。
疼痛:胰腺癌比较常见的并发症之一,可以在手术过程中进行放射治疗或者进行经皮给药及内脏的神经阻滞,改善患者的疼痛的症状。
体重减轻:比较多见,患者发病后短期内出现明显的消瘦,伴有衰弱、乏力的情况。
症状性糖尿病:少数病人起病的时候最初表现就是糖尿病症状,因此糖尿病患者出现持续性的腹痛或者老年人突然出现糖尿病,或者在原来糖尿病的基础上突然出现病情加重,都应该警惕发生胰腺癌的可能。
血栓性静脉炎:晚期胰腺癌患者可以出现游走性的血栓性静脉炎或者动脉性的血栓形成。
精神方面的症状:部分胰腺癌患者可表现为焦虑、急躁、抑郁、个性改变等精神症状。
1、初步评估
症状询问:重点关注腹痛、黄疸、体重下降、消化不良等典型表现。
高危人群筛查:长期吸烟、慢性胰腺炎、糖尿病、家族史(如 BRCA1/2 突变)、肥胖等人群需加强监测。
2、血液检查
肿瘤标志物:CA19-9,最常用,敏感性约 80%,但特异性不足(胆管炎、胰腺炎时也可能升高); CEA,约 30% 患者升高,可辅助判断预后。
肝功能:胆红素升高提示胆道梗阻,ALP、GGT 升高支持梗阻性黄疸。
血糖 / 糖化血红蛋白:部分患者合并糖尿病或糖耐量异常。
3、影像学检查
CT 平扫 + 增强:首选筛查方法,可显示肿瘤位置、大小、周围侵犯及淋巴结转移(如胰头癌侵犯胆总管、门静脉)。
MRI/MRCP:对胰腺实质和胆道系统分辨率更高,适用于 CT 显示不清或怀疑肝转移者。
超声内镜(EUS):可发现 < 1cm 的微小肿瘤,引导细针穿刺(EUS-FNA)获取组织标本。
ERCP:用于胆道梗阻时放置支架,同时可获取胆汁细胞学检查。
4、病理活检
EUS-FNA:通过超声内镜引导穿刺肿瘤,准确率 > 90%,是确诊金标准。
手术探查活检:适用于疑似可切除肿瘤但穿刺阴性者,术中快速冰冻切片明确诊断。
胰腺癌的病因复杂,是遗传、环境和生活方式等多因素长期共同作用的结果。
【家族史】
约 5%~10% 的胰腺癌患者有家族聚集性,若一级亲属(父母、子女、兄弟姐妹)中有 1 人患胰腺癌,个体风险增加 2~3 倍;若有 2 人患病,风险升至 5~7 倍。
【遗传性综合征】
BRCA1/2 突变:乳腺癌 / 卵巢癌相关基因,突变者胰腺癌风险显著升高(BRCA2 突变风险约 5%~10%)。
遗传性胰腺炎:PRSS1 基因突变导致的慢性胰腺炎,患者 20 年胰腺癌累积风险约 40%。
Peutz-Jeghers 综合征:STK11 基因突变,胃肠道息肉伴黏膜黑斑,胰腺癌风险增加 132 倍。
家族性非典型多痣黑素瘤综合征(FAMMM):CDKN2A 基因突变,胰腺癌风险增加 17 倍。
【吸烟】
吸烟是胰腺癌首要危险因素,吸烟者风险比非吸烟者高 2~3 倍,且呈剂量依赖性(每日吸烟量越多、时间越长,风险越高)。
机制:烟草中的多环芳烃、亚硝胺等致癌物通过血液进入胰腺,诱发 DNA 损伤。
【饮食与肥胖】
高风险饮食:高脂肪、高胆固醇、红肉(如加工肉类)摄入过多,可能促进胰腺炎症和细胞增殖。
肥胖:BMI≥30 的人群胰腺癌风险增加 30%~50%,可能与胰岛素抵抗和慢性炎症相关。
【慢性胰腺炎】
反复发作的慢性胰腺炎(尤其是酒精性或遗传性胰腺炎)导致胰腺纤维化和导管上皮化生,癌变风险显著增加(年风险约 1%)。
【糖尿病】
长期糖尿病:病程≥10 年者风险升高 20%~50%,高血糖可能促进胰腺细胞异常增殖。
新发糖尿病:50 岁以上无诱因的糖尿病需警惕胰腺癌,可能是肿瘤破坏胰岛 β 细胞的早期表现。
【胆道疾病】
胆总管结石、胆管炎等导致胆汁淤积,可能增加胰管损伤和癌变风险。
【职业暴露】
长期接触芳香胺(如染料、橡胶工业)、亚硝胺(如皮革加工)、重金属(如镍、铬)等化学物质。
【年龄与性别】
发病高峰在 60~80 岁,男性略多于女性(可能与吸烟、饮酒习惯相关)。
胰腺癌(尤其是胰腺导管腺癌,PDAC)的分子生物学致病机制是一个多步骤、多因素参与的复杂过程,涉及关键基因突变、信号通路异常、表观遗传失调、代谢重编程及独特的肿瘤微环境(TME)特征。其以早期转移、治疗抵抗和极低生存率为特点,分子机制研究对开发新疗法至关重要。
1、关键基因突变与分子分型
胰腺癌的基因组特征以高频驱动基因突变为核心,主要分为以下四类:
【KRAS突变】
突变频率:>90%的PDAC存在KRAS突变(多为G12D、G12V、G12R),导致持续激活下游信号(MAPK、PI3K/AKT),驱动细胞增殖、代谢重编程和免疫逃逸。
功能影响:KRAS突变促进自噬激活、肿瘤干细胞特性维持及间质纤维化。
【TP53失活】
约75%病例存在TP53突变或缺失,导致基因组不稳定性、细胞周期失控和凋亡抵抗。
【CDKN2A(p16)缺失】
约90%病例中CDKN2A基因失活(突变、缺失或甲基化),解除对细胞周期(G1/S期)的抑制作用。
【SMAD4(DPC4)缺失】
约50%病例发生SMAD4突变或缺失,导致TGF-β信号通路失调,促进EMT(上皮-间质转化)和转移。
【其他基因】
DNA修复基因:BRCA1/2、PALB2等同源重组修复(HRR)缺陷(约10%病例),增加对铂类化疗和PARP抑制剂的敏感性。
表观调控基因:MLL3、ARID1A等染色质重塑基因突变影响分化程序。
2、信号通路异常
【KRAS下游通路】
MAPK/ERK通路:促进细胞增殖和存活。
PI3K/AKT/mTOR通路:调控代谢重编程(如糖酵解增强)和抗凋亡。
RALGEF通路:介导细胞迁移和膜运输。
TGF-β/SMAD通路:SMAD4存在时,TGF-β发挥抑癌作用;SMAD4缺失后,TGF-β通过非经典通路(如MAPK)促进侵袭。
Hedgehog(HH)通路:间质细胞中SHH过表达,通过旁分泌作用激活成纤维细胞,促进间质纤维化和免疫抑制。
Notch通路:异常激活维持肿瘤干细胞特性并诱导化疗耐药。
3、表观遗传学调控异常
DNA甲基化:抑癌基因(如CDKN2A、SPARC)启动子高甲基化导致沉默;促转移基因(如S100A4)低甲基化激活。
组蛋白修饰:EZH2过表达(Polycomb组蛋白甲基转移酶)抑制分化相关基因(如INK4a/ARF),促进干性。
非编码RNA:
miRNA:miR-21抑制PTEN促进增殖;miR-34a缺失增强EMT。
lncRNA:HOTAIR通过结合PRC2复合体沉默抑癌基因;PANDA调控细胞周期和凋亡。
4、肿瘤微环境(TME)与免疫逃逸
胰腺癌的TME以纤维化间质(占肿瘤体积80%)和免疫抑制为特征。
【间质重塑】
癌症相关成纤维细胞(CAF):分泌胶原、纤连蛋白和生长因子(如HGF、FGF),促进肿瘤生长和化疗抵抗。
细胞外基质(ECM)硬化:通过整合素信号激活YAP/TAZ通路,驱动细胞增殖。
【免疫抑制】
髓源性抑制细胞(MDSC)和调节性T细胞(Treg):分泌IL-10、TGF-β,抑制CD8+T细胞活性。
肿瘤相关巨噬细胞(TAM-M2型):通过PD-L1表达和精氨酸酶(ARG1)诱导免疫耐受。
低免疫原性:肿瘤突变负荷(TMB)低,新抗原稀少,导致免疫检查点抑制剂(如PD-1抑制剂)疗效有限。
5、代谢重编程与氧化应激
自噬依赖:KRAS突变细胞依赖自噬清除受损细胞器并提供代谢底物,自噬抑制剂(如羟氯喹)在临床试验中。
谷氨酰胺成瘾:谷氨酰胺通过谷氨酰胺酶(GLS1)转化为α-酮戊二酸,支持TCA循环和核苷酸合成。
糖酵解增强:Warburg效应显著,上调GLUT1、HK2和LDHA,乳酸堆积进一步酸化微环境促进侵袭。
脂代谢异常:脂肪酸氧化(FAO)增强提供能量;胆固醇合成酶(如HMGCR)过表达支持膜合成。
6、慢性炎症与癌变
胰腺炎-癌变轴:慢性胰腺炎导致炎症因子(如TNF-α、IL-6)释放,激活NF-κB和STAT3通路,促进细胞增殖和基因组损伤。炎症微环境中ROS/RNS累积诱导DNA突变(如KRAS早期激活)。
微生物组影响:肠道菌群失调可能通过调节免疫应答或代谢产物(如次级胆汁酸)促进胰腺癌进展。
胰腺癌的治疗需根据分期、病理类型及患者全身状况制定个体化方案,以手术切除为核心,结合放化疗、靶向治疗及免疫治疗等综合手段。
1、根治性手术
适应症:早期肿瘤(T1-T2,无远处转移,未侵犯大血管)。
【术式】
胰十二指肠切除术(Whipple 术):适用于胰头癌。
胰体尾切除术:适用于胰体尾癌。
全胰切除术:罕见,用于多灶性肿瘤或广泛侵犯。
预后:R0 切除(切缘阴性)患者 5 年生存率约 20%-30%,但术后复发率高(约 80%)。
2、姑息性手术
目的:缓解梗阻性黄疸、十二指肠梗阻或疼痛。
【术式】
胆总管空肠吻合术:解除胆道梗阻。
胃空肠吻合术:解除十二指肠梗阻。
1、新辅助化疗
适用人群:局部晚期可切除或临界可切除患者(如 T3,未侵犯腹腔干 / SMA)。
【方案】
FOLFIRINOX(5-FU + 亚叶酸钙 + 伊立替康 + 奥沙利铂):推荐用于体力状态良好者。
吉西他滨 + 白蛋白紫杉醇:耐受性较好。
目标:缩小肿瘤、降期以提高手术切除率。
2、辅助化疗
适用人群:术后病理提示淋巴结转移、切缘阳性或高危因素(如低分化、血管侵犯)。
【方案】
吉西他滨单药:经典方案,延长无病生存期。
CAPEOX(卡培他滨 + 奥沙利铂):近年推荐用于高危患者。
3、晚期一线化疗
【方案】
FOLFIRINOX:中位总生存期(OS)11.1 个月,PS 评分好者首选。
吉西他滨 + 白蛋白紫杉醇:OS 8.5 个月,耐受性更佳。
二线治疗:以 5-FU 为基础的方案(如 FOLFOX)或靶向药物。
适应症:局部晚期不可切除患者(联合化疗); 术后辅助放疗(切缘阳性或淋巴结转移); 寡转移灶姑息治疗。
技术:调强放疗(IMRT),精准照射肿瘤,减少正常组织损伤;立体定向放疗(SBRT),用于寡转移灶或复发病灶。
疗效:同步放化疗(如吉西他滨 + 放疗)可延长局部控制时间。
【KRAS G12C 抑制剂】
Sotorasib:2022 年 FDA 批准用于 KRAS G12C 突变的晚期胰腺癌(客观缓解率 12%,中位 PFS 4.0 个月)。
Adagrasib:临床试验显示中位 OS 6.5 个月。
【抗血管生成药物】
阿帕替尼:联合化疗可能改善疗效,但需警惕出血风险。
【HER2 靶向治疗】
曲妥珠单抗:仅适用于 HER2 过表达的罕见亚型(如导管腺癌伴 HER2 扩增)。
【PD-1/PD-L1 抑制剂】
帕博利珠单抗:单药疗效有限(客观缓解率<5%),需联合化疗或放疗。
纳武利尤单抗 + 伊匹木单抗:在 MSI-H/dMMR 型胰腺癌中有效率约 50%。
挑战:胰腺癌免疫微环境高度抑制(Tregs 浸润、MDSCs 聚集),需联合免疫调节剂。
胆道引流:内镜下放置支架解除黄疸(成功率>90%)。
疼痛管理:阿片类药物 + 区域神经阻滞(如腹腔神经丛毁损术)。
营养支持:肠内营养为主,必要时肠外营养。
心理支持:改善焦虑抑郁状态,提高生活质量。
溶瘤病毒:如 ONCOS-102 联合 PD-1 抑制剂,激活抗肿瘤免疫。
CAR-T 细胞治疗:靶向 Claudin 18.2 的临床试验正在进行。
肿瘤疫苗:GVAX 疫苗联合免疫检查点抑制剂显示潜力。
本病属于伏梁、痛、黄痘、积聚、等范畴。中医认为,本病与肝脾胃关密切, 主要病因病机为七情内伤、外邪侵袭、饮食失宜,致脾损伤、脏腑失和、 湿毒内蕴、气滞血瘀日久而形成本病,本病之病因病机以气血痰湿互阻, 湿热邪毒内攻,脾胃与阴两虚为特点,故其治疗则当行气活血、化痰散结 以祛其邪益气健脾、养阴和胃以补其虚。常用辨证与辨病相结合,再随症 加减的方法。
【辨证用方】
1.湿浊阻遏证
【主症】胸脘痞闷,头重身困,恶心欲呕,纳呆,腹部隐痛,身目俱黄, 黄色晦暗,口于不欲饮,大便溏薄,舌质淡苔白腻,脉沉细或沉迟。
【治法】健脾利湿,化浊解毒。
【主方】加减茵陈五苓散(《中华肿瘤治疗大成》)
【组成与用法】茵陈30g,猪苓12g,茯苓12g,白术10g,泽泻15g,桂枝10g, 菝葜20g,陈皮10g,法半夏10g,石则穿30g,山慈菇30g,甘草5g。水煎服。
【功能主治】利湿化浊解毒。主治胰腺癌。
【加减应用】脾阳不振,寒湿阻遏明显者,加制附片、千姜;湿邪郁而化热者,加藿香、黄苓、苡仁。
2.气血瘀滞证
【主症】脘腹胀满,恶心呕吐或呃逆,上腹疼痛呈持续性、务处固定,腹中痞块, 而目发黄而晦黯,形体消瘦、舌质青紫,或有瘀斑,苔薄,脉弦细或涩。
【治法】行气化瘀,软坚散结。
【主方】加减膈下逐瘀汤(《中华肿瘤治疗大成》)
【组成与用绣】五灵脂(布包)10g,制香附12g,乌药9g,延胡索30g,红花10g, 桃仁10g,生地12g,赤芍15g,积壳10g,紫丹参30g,炮山甲(先煎)10g, 茵陈20g,八月札10g,浙贝母15g,菝葜30g,藤梨根30g,甘草5g,水煎服。
【功能主治】理气活血,化瘀解毒。主治胰腺癌。
【加减应用】病程迁延,而见纳差、乏力者,去五加白术、茯苓、党参、陈皮; 瘀血内结较甚者,加川楝子、山棱、莪术;腹胀明显者,加隔山消、沉香粉、大腹皮。
3.肝郁蕴热证
【主症】脘胁胀满,腹痛拒按,身目发黄,纳呆,暖气恶心,烦躁易怒,发热, 小便黄赤,大便干结,舌质红而燥,苔黄厚腻,脉弦数或滑数。
【治法】疏肝解郁,清热解毒。
【主方】加减柴胡疏肝散(《中华肿瘤治疗大成》)
【组成与用法】柴胡10g,杭白芍30g,制香附15g,枳壳10g,川芎6g, 白花蛇舌草30g,两面针30g,土茯苓30g,白毛藤30g,垂盆草30g,虎杖30g, 菝葜30g,甘草5g。水煎服。
【功能主治】疏肝理气,清热解毒。主治胰腺癌。
【加减应用】兼瘀象者,加延胡索、莪术;黄疽明显,终痛牵引肩背, 或恶寒发热,大便色淡灰白者,加茵陈、金钱草、郁金、栀子。
4.气血亏损证
【主症】腹胀隐痛,扪及包块,纳差、倦怠乏力,全身消发,面色萎黄,舌质淡, 或有瘀点、瘀斑,苔薄白,脉沉细。
【治法】益气养血,化瘀散结。
【主方】加减十全大补汤(《中华肿瘤治疗大成》)
【组成与用法】生黄芪15g,潞党参15g,全当归15g,炒白术12g,大熟地15g, 茯苓15g,猪苓15g,鸡血藤30g,炙鳖甲(先煎)9g,枸杞子12g,浙贝母15g, 炮山甲(先煎)10g,蚤休30g,甘草6g。水煎服。
【功能主治】补益气血,化瘀软坚。主治胰腺痛
【加减应用】兼脾虚湿困者,加薏苡仁、砂仁、陈皮、法半夏;积块日久、 阴伤甚而见舌红无苔、脉细数者,加生地、北沙参、石斛;呕血,便血者,加槐花、 地榆炭、大黄粉。
胰腺癌的生存期受肿瘤分期、治疗方案、患者体能状态及生物学特性等因素影响,总体预后较差,但近年随着精准治疗的发展,部分患者生存期有所改善。
根据AJCC 第 8 版分期,胰腺癌 5 年生存率如下:
I 期(肿瘤局限于胰腺):20%-30%
II 期(侵犯周围组织 / 淋巴结):10%-20%
III 期(侵犯大血管或区域淋巴结转移):<5%
IV 期(远处转移):<1%
中位总生存期(OS):
晚期(转移性)患者:约1 年(一线化疗方案如 FOLFIRINOX 或吉西他滨 + 白蛋白紫杉醇)。
局部晚期不可切除患者:约14-18 个月(同步放化疗)。
早期可切除患者:术后中位 OS 为18-24 个月,5 年生存率仅 20%-30%。
胰腺癌的预防需针对高危因素采取措施,而护理则需贯穿治疗全程,注重症状管理、生活质量提升及心理支持。
1、控制高危因素
戒烟:吸烟是胰腺癌首要可预防风险,吸烟者风险比非吸烟者高 2-3 倍。
健康饮食:减少红肉、加工食品摄入,增加蔬菜(如西兰花、菠菜)、水果(柑橘类)及全谷物摄入。
限酒:男性每日酒精摄入 < 25g,女性 < 15g。
2、管理慢性疾病
糖尿病:长期高血糖增加胰腺癌风险,需严格控制血糖。
肥胖:BMI 控制在 18.5-24.9。
胰腺炎:反复发作的慢性胰腺炎患者需定期筛查。
3、筛查与监测
高危人群(如家族性腺瘤性息肉病、BRCA1/2 突变携带者): 40 岁起每年进行一次 CT/MRI 或内镜超声(EUS)筛查。
普通人群:45 岁以上建议每 2-3 年检测 CA19-9 和 CEA 肿瘤标志物,结合腹部超声初筛。
1、术前护理
营养支持:术前纠正贫血、低蛋白血症,必要时肠内营养管饲。
心理疏导:缓解手术焦虑,讲解术后康复流程。
2、术后护理
引流管管理:观察胰瘘、胆瘘等并发症,保持引流管通畅。
疼痛控制:阶梯式用药(非甾体抗炎药→弱阿片→强阿片),必要时神经阻滞。
3、症状管理
消化功能障碍:胰酶替代治疗(如胰酶肠溶胶囊),低脂饮食。
黄疸:PTCD 引流或支架置入术改善肝功能。
恶液质:高蛋白饮食 + 甲地孕酮促进食欲,必要时静脉营养。
4、化疗 / 放疗护理
骨髓抑制:监测血常规,粒细胞缺乏期预防感染。
手足综合征:穿软底鞋,避免摩擦,局部冷敷。
放射性肠炎:低脂少渣饮食,止泻药(如蒙脱石散)。
5、心理与社会支持
心理干预:认知行为疗法(CBT)缓解焦虑抑郁,必要时抗抑郁药(如舍曲林)。
社会资源:加入患者互助小组,申请医疗救助(如中国癌症基金会资助项目)。
6、随访与复发监测
术后前 2 年:每 3 个月复查 CA19-9、CT/MRI,监测复发。
晚期患者:每月评估疼痛评分(NRS)、KPS 体力状态评分,调整治疗方案。
7、老年患者护理
优先选择毒性较低的化疗方案(如吉西他滨单药),密切监测肾功能。必要时进行跌倒风险评估,补充维生素 D 预防骨质疏松。
胰腺癌患者的饮食保健应该综合考虑营养均衡、易消化和低脂肪等原则,以支持患者的治疗和康复。
1、增加新鲜蔬菜、新鲜水果的摄入
2、选择易消化的碳水化合物
3、增加富含Omega-3脂肪酸的食物: 如三文鱼、鲭鱼等,具有抗炎作用。
4、避免刺激性食物
5、保持饮食卫生
6、少量多餐
7、避免高脂肪食物
8、保持充足的水分摄入
1、黄芪枸杞乌鸡汤
【材料】黄芪 30g、枸杞 15g、乌鸡半只、生姜 3 片。
【做法】乌鸡焯水后与药材同炖 2 小时,加盐调味。
【功效】补气养血,适合术后气血虚弱者。
2、茯苓山药粥
【材料】茯苓 20g、山药 50g、粳米 100g。
【做法】茯苓研粉,与山药、粳米煮粥。
【功效】健脾利湿,缓解术后腹胀、食欲不振。
3、姜枣小米粥
【材料】生姜 5 片、红枣 5 颗、小米 50g。
【做法】小米煮至软烂,加入姜枣煮 10 分钟。
【功效】温中和胃,缓解化疗引起的恶心。
4、五红汤
【材料】红豆 30g、红皮花生 30g、红枣 5 颗、枸杞 10g、红糖适量。
【做法】食材煮烂后加红糖调味。
【功效】补血升白,改善骨髓抑制。
5、蒲公英茶
【材料】干蒲公英 10g。
【做法】沸水冲泡代茶饮。
【功效】清热解毒,辅助抑制肿瘤细胞。
6、姜黄鸡丝饭
【材料】鸡胸肉 100g、姜黄粉 5g、胡萝卜半根、大米 100g。
【做法】鸡丝炒香后与姜黄、胡萝卜同焖饭。
【功效】姜黄素抑制炎症通路,适合长期食用。
7、石榴皮山药汤
【材料】石榴皮 15g、山药 30g。
【做法】煮水。
【功效】收敛止泻。
8、黑芝麻蜂蜜饮
【材料】黑芝麻 30g。
【做法】研磨,加蜂蜜温水冲服。
【功效】润肠通便。
9、百合莲子银耳羹
【材料】百合 20g、莲子 15g、银耳 10g。
【做法】煮羹
【功效】宁心安神。
备注:更多食疗方见肿瘤药膳专栏,或点击本页相关文章栏目相应文章链接阅读。