脑癌(Brain Cancer)是指起源于脑组织或中枢神经系统(CNS)的恶性肿瘤, 占全身肿瘤的1%-2%,但因其位置特殊、侵袭性强且治疗难度大, 致死率和致残率极高。近年来,随着诊疗技术进步和分子分型的应用, 脑癌的个体化治疗逐渐成为研究热点,但其发病机制复杂,早期诊断仍面临巨大挑战。
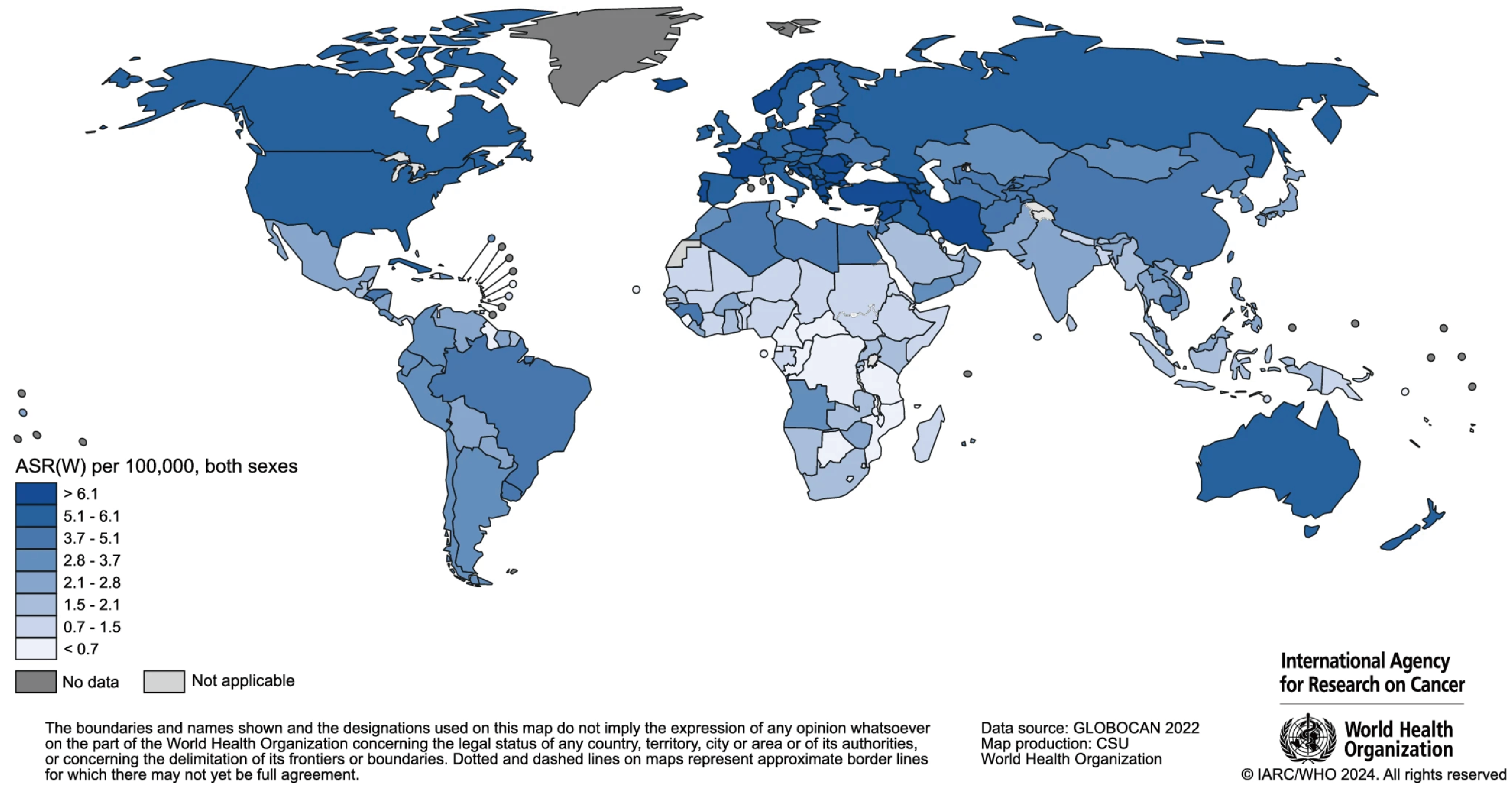
图1.显示了基于五分位数的脑和中枢神经系统肿瘤的估计年龄标准化发病率 [1]。
在世界范围内,2022年估计有30.8万例新病例,其中西欧和北美的总体发病率最高。 在儿童中,北美洲的发病率最高,其次是南欧和澳大利亚/大洋洲。 大多数新病例和最高发病率发生在40岁及以上的人群中,其中欧洲地区的发病率最高 [1]。 2022年,全球约25万人死于脑癌 [2]。
2022年,中国脑癌新发病例约8.75万例,其中男性病例约4.24万例,女性病例约4.51万例。 同年,中国脑癌死亡病例约5.66万例,其中男性病例约3.16万例,女性病例约2.51万例 [3]。
脑癌(Brain Cancer)是指起源于脑组织或中枢神经系统(CNS)的恶性肿瘤,包括原发性脑癌(原发于脑或脊髓)和 转移性脑癌(由其他器官肿瘤转移至脑)。
原发性脑癌:起源于神经胶质细胞、神经元、脑膜、垂体或神经鞘等结构,具有高度侵袭性。
转移性脑癌:占所有脑肿瘤的50%以上,常见原发灶为肺癌(40%-50%)、乳腺癌(15%-20%)、黑色素瘤等。
根据世界卫生组织(WHO)2021年中枢神经系统肿瘤分类(第五版),脑癌按组织来源、分子特征及临床行为分为以下主要类型:
1、神经上皮组织肿瘤(胶质瘤为主)
占原发性脑癌的70%-80%,起源于神经胶质细胞,按恶性程度分为低级别(I-II级) 和高级别(III-IV级)。
【星形细胞肿瘤】
低级别:
毛细胞型星形细胞瘤(I级):儿童小脑常见,预后较好。
弥漫性星形细胞瘤(II级):成人多见,IDH突变型,中位生存期5-10年。
高级别:
间变性星形细胞瘤(III级):IDH突变型,易复发。
胶质母细胞瘤(GBM,IV级):
IDH野生型:占90%,中位生存期12-15个月。
IDH突变型:罕见,预后稍好(生存期约2-3年)。
【少突胶质细胞肿瘤】
少突胶质细胞瘤(II级):1p/19q共缺失,IDH突变,对化疗敏感。
间变性少突胶质细胞瘤(III级):进展快,但生存期优于GBM。
【室管膜肿瘤】
室管膜瘤(II-III级):儿童后颅窝常见,分子分型(如RELA融合)。
间变性室管膜瘤(III级):恶性度高,易复发。
【神经元和混合性神经元-胶质肿瘤】
节细胞胶质瘤(I级):儿童/青年,癫痫为典型症状。
髓母细胞瘤(IV级):儿童小脑高发,分WNT型、SHH型等分子亚型,预后差异大。
2、脑膜肿瘤
起源于脑膜,多数为良性,但恶性脑膜瘤占10%-15%。
良性脑膜瘤(I级):生长缓慢,手术可治愈。
非典型脑膜瘤(II级):复发风险高,需术后放疗。
间变性/恶性脑膜瘤(III级):侵袭性强,预后差。
3、神经鞘瘤与神经纤维瘤
听神经瘤(前庭神经鞘瘤):良性,与NF2基因相关,可致听力丧失。
恶性周围神经鞘瘤(MPNST):罕见,恶性度高,与NF1综合征相关。
4、垂体与松果体肿瘤
垂体腺瘤:多为良性,分功能型(分泌激素)和无功能型。
松果体母细胞瘤:高度恶性,儿童多见。
5、淋巴瘤和生殖细胞肿瘤
原发性中枢神经系统淋巴瘤(PCNSL)
多与免疫功能抑制(如HIV)相关,弥漫大B细胞型为主。
生殖细胞肿瘤
生殖细胞瘤:对放化疗敏感,预后较好。
非生殖细胞瘤性生殖细胞肿瘤(NGGCT):如畸胎瘤、卵黄囊瘤,恶性度高。
6、转移性脑癌
常见来源:肺癌、乳腺癌、黑色素瘤、肾癌、结直肠癌。
特点:多发性病灶,周围水肿明显,治疗以放疗、靶向或免疫治疗为主。
脑癌的症状和体征因肿瘤的大小、位置及恶性程度而异,常见的症状和体征包括:
1、颅内压增高症状
头痛:持续性或阵发性加剧,常在早晨更重,可能伴有搏动感。
恶心和呕吐:频繁呕吐,通常发生在头痛之后,可能伴有恶心感。
视力障碍:视力模糊、视野缺损、复视等,严重时可能导致失明。
精神及意识障碍:头晕、意识模糊、精神不安或淡漠,可能伴有癫痫发作。
2、局限性症状
精神症状:反应迟钝、生活懒散、记忆力减退,严重时可能丧失自知力及判断力。
癫痫发作:全身大发作或局限性发作,以额叶最为多见。
锥体束损害症状:肿瘤对侧半身或单一肢体力弱或瘫痪,病理征阳性。
感觉障碍:肿瘤对侧肢体的位置觉、两点分辨觉、图形觉、质料觉、实体觉的障碍。
视野改变:视野缺损,偏盲。
3、特定部位症状
蝶鞍区肿瘤:视觉障碍、内分泌功能紊乱,如性腺功能低下、肢端肥大症等。
四叠体受压迫症状:视障碍、瞳孔对光反应和调节反应障碍、耳鸣、耳聋、共济失调、尿崩症等。
颅后窝肿瘤:小脑半球症状(共济失调、眼球震颤等)、小脑蚓部症状(躯干性和下肢远端的共济失调)、脑干症状(交叉性麻痹等)。
小脑桥脑角症状:耳鸣、听力下降、眩晕、面肌麻痹、声音嘶哑等。
脑癌的并发症因肿瘤的生长和治疗的影响而异,常见的并发症包括:
1、颅内压增高
脑肿瘤生长导致颅内压增高,可能引起头痛、呕吐、视力模糊等症状,严重时可能导致脑疝。
2、癫痫发作
脑癌患者可能出现癫痫发作,影响日常生活和安全。
3、感染
脑肿瘤患者免疫力下降,容易发生感染,如脑膜炎、肺炎等。
4、脑水肿
脑肿瘤周围组织可能出现水肿,加重颅内压增高,需要使用皮质类固醇等药物治疗。
5、脑积水
脑肿瘤可能压迫脑室系统,导致脑脊液循环不畅,形成脑积水。
6、肢体功能障碍
脑癌可能导致肢体无力、麻木或瘫痪,影响患者的活动能力。
7、认知功能下降
脑癌晚期患者可能出现认知功能下降,如记忆力减退、注意力不集中、思维迟缓等。
8、精神和心理问题
脑癌患者可能出现精神异常,如抑郁、焦虑、人格改变等,需要心理支持和治疗。
脑癌的诊断需结合影像学检查、病理学分析及分子生物学检测,旨在明确肿瘤性质、分级及指导治疗。
磁共振成像(MRI):
首选方法:对软组织分辨率高,可清晰显示肿瘤位置、大小及与周围结构关系。
增强MRI:注射钆造影剂后,恶性脑瘤多呈不均匀强化(如胶质母细胞瘤的“花环样”强化)。
功能MRI(fMRI):定位肿瘤与运动/语言功能区的关系,指导手术规划。
计算机断层扫描(CT):
适用场景:急诊快速排查出血或钙化(如脑膜瘤钙化)、无法接受MRI者(如体内金属植入物)。
局限性:对低级别胶质瘤或微小转移灶敏感性较低。
正电子发射断层扫描(PET-CT):
原理:利用放射性示踪剂(如¹⁸F-FDG)检测肿瘤代谢活性,鉴别肿瘤复发与放射性坏死。
联合MRI:提高胶质瘤分级准确性(高级别肿瘤代谢活性更高)。
组织活检:
立体定向穿刺活检:适用于深部或功能区肿瘤,通过三维坐标精准取样。
术中冰冻病理:指导手术范围(如区分胶质瘤与炎性病变)。
病理分型与分级:
WHO分级:根据细胞异型性、增殖活性(如Ki-67指数)分为Ⅰ~Ⅳ级。
分子标志物: IDH1/2突变:提示预后较好(低级别胶质瘤常见)。
MGMT启动子甲基化:预测胶质母细胞瘤对替莫唑胺的敏感性。
1p/19q共缺失:少突胶质细胞瘤的诊断标志,提示化疗敏感。
脑脊液(CSF)分析:腰椎穿刺:检测脑脊液压力、细胞学(如淋巴瘤或转移瘤的癌细胞)、蛋白及葡萄糖水平。
禁忌症:严重颅内压增高者需谨慎(可能诱发脑疝)。
血液肿瘤标志物:非特异性指标:如β-HCG(生殖细胞瘤)、AFP(卵黄囊瘤)。
循环肿瘤DNA(ctDNA):研究阶段,用于监测复发或耐药突变。
脑电图(EEG):
适用性:癫痫发作患者定位异常放电区域,辅助鉴别肿瘤与癫痫灶。
血管造影(DSA/MRA):
评估血供:明确肿瘤与血管关系(如脑膜瘤的“脑膜尾征”)。
术前栓塞:减少富血供肿瘤(如血管母细胞瘤)术中出血。
全身影像筛查:
胸部CT:排查肺癌(最常见原发灶)。
乳腺钼靶/超声:女性患者排除乳腺癌转移。
全身PET-CT:寻找隐匿原发灶。
病理溯源:转移瘤与原发癌的免疫组化标志对比(如TTF-1提示肺癌,ER/PR提示乳腺癌)。
脑癌(恶性脑肿瘤)的病因复杂,通常由遗传、环境及生活方式等多因素共同作用引发。目前明确的致病因素较少,但以下风险因素与脑癌的发生密切相关。
1、电离辐射
高剂量辐射暴露:
儿童时期接受头部放射治疗(如白血病放疗)显著增加成年后胶质瘤、脑膜瘤风险。
核事故或职业性辐射暴露(如放射科医生未规范防护)。
机制:辐射直接损伤DNA,引发基因突变或表观遗传改变。
2、遗传性肿瘤综合征
神经纤维瘤病1型(NF1):增加胶质瘤(尤其是视神经胶质瘤)风险。
李-弗劳梅尼综合征(Li-Fraumeni):TP53基因突变,易患胶质母细胞瘤、髓母细胞瘤。
结节性硬化症(TSC):诱发室管膜下巨细胞星形细胞瘤(SEGA)。
遗传性视网膜母细胞瘤:RB1基因突变,增加松果体母细胞瘤风险。
3、免疫抑制状态
艾滋病、器官移植后:免疫功能低下者患原发性中枢神经系统淋巴瘤(PCNSL)风险升高。
4、EB病毒感染:与PCNSL发病相关(常见于免疫抑制人群)。
环境化学物质
长期接触致癌物:有机溶剂(如苯)、杀虫剂(农业从业者)、石油化工产品(橡胶、塑料行业)。甲醛(装修材料)可能与胶质瘤相关,但需更多研究证实。
电磁场暴露
手机与无线设备:长期高频使用手机(≥10年)可能与同侧听神经鞘瘤、胶质瘤风险轻度升高相关(WHO列为2B类可能致癌物)。儿童及青少年因颅骨较薄,脑组织吸收辐射量更高,需谨慎使用。
创伤与慢性炎症
头部外伤:脑膜瘤风险可能增加(创伤后修复过程中细胞异常增生)。
慢性脑炎或感染:如弓形虫、巨细胞病毒(CMV)感染可能与部分肿瘤相关。
激素与代谢因素
雌激素:脑膜瘤在女性中更常见,可能与激素受体(如孕激素受体)表达有关。
肥胖与糖尿病:代谢异常或促进肿瘤微环境形成(证据有限)。
(三)年龄与性别差异
年龄
儿童:胚胎性肿瘤(髓母细胞瘤)、低级别胶质瘤为主。
成人:胶质母细胞瘤、脑膜瘤高发,50~70岁为发病高峰。
性别
男性:胶质瘤、垂体瘤发病率略高于女性。
女性:脑膜瘤、听神经鞘瘤更常见。
(四)其他可能关联因素
饮食与生活方式
亚硝基化合物:腌制食品(含亚硝酸盐)可能增加儿童脑瘤风险(研究尚不充分)。
维生素D缺乏:低水平维生素D与胶质瘤风险升高相关(需进一步验证)。
过敏与免疫反应
过敏史:部分研究表明过敏体质者胶质瘤风险降低,机制可能与免疫监测增强有关。
脑癌的分子生物学致病机制具有高度异质性和复杂性,涉及基因突变、表观遗传失调、信号通路异常、肿瘤微环境重塑及代谢重编程等多层次调控失衡。
1、关键基因突变与分子分型
脑癌的分子特征因病理类型而异(如胶质瘤、髓母细胞瘤、脑膜瘤),以胶质母细胞瘤(GBM)为例:
【IDH1/2突变】
IDH1 R132H(继发性GBM常见):突变酶催化α-酮戊二酸(α-KG)生成致癌代谢物2-羟基戊二酸(2-HG),抑制组蛋白去甲基化酶(如KDM4)和TET家族DNA去甲基化酶,导致全局性高甲基化(G-CIMP表型),促进分化阻滞和肿瘤发生。
【EGFR扩增/突变】
EGFRvIII(原发性GBM常见):组成性激活的截短型受体,持续激活下游PI3K/AKT/mTOR和RAS/MAPK通路,驱动增殖和侵袭。
【TP53与PTEN缺失】
TP53突变(>80%继发性GBM):导致基因组不稳定性;
PTEN缺失(约40% GBM):解除对PI3K通路的抑制,促进代谢重编程。
【TERT启动子突变】
端粒酶活性异常升高,赋予肿瘤细胞无限增殖能力。
【1p/19q共缺失】
少突胶质细胞瘤标志,提示对化疗敏感(替莫唑胺)。
2、关键信号通路异常
RTK/RAS/PI3K通路:EGFR、PDGFR等受体酪氨酸激酶(RTK)异常激活,通过RAS-MAPK和PI3K-AKT-mTOR级联促进增殖、存活和血管生成。
Notch通路:激活Notch信号维持胶质瘤干细胞(GSCs)自我更新,与放疗抵抗相关。
Wnt/β-catenin通路:异常激活促进上皮-间质转化(EMT)和侵袭(尤其在间充质型GBM中)。
Hedgehog通路:髓母细胞瘤的核心驱动通路(如PTCH1突变),调控细胞周期和干细胞特性。
3、表观遗传学调控异常
【DNA甲基化】
MGMT启动子甲基化:沉默DNA修复酶MGMT,增强替莫唑胺疗效;
G-CIMP表型(IDH突变型):全基因组高甲基化抑制分化相关基因。
【组蛋白修饰】
H3K27M突变(儿童弥漫中线胶质瘤):抑制PRC2复合体功能,降低H3K27me3水平,激活致癌基因转录。
EZH2过表达:通过H3K27me3修饰沉默抑癌基因,促进干细胞特性。
【非编码RNA】
miR-21:抑制PTEN和PDCD4,促进增殖和侵袭;
lncRNA H19:通过IGF2印记调控促进血管生成。
4、肿瘤微环境(TME)与免疫逃逸
血脑屏障(BBB)与免疫豁免:BBB限制免疫细胞浸润,但肿瘤相关巨噬细胞(TAM)和小胶质细胞主导免疫抑制微环境,分泌IL-10、TGF-β等抑制T细胞活性。
缺氧与血管生成:缺氧诱导因子HIF-1α激活VEGF、CXCR4等基因,促进血管异常增生(“血管共选择”现象)。
细胞外基质(ECM)重塑:胶质瘤细胞分泌tenascin-C和MMP-9,破坏正常脑组织并促进侵袭。
5、代谢重编程与氧化应激
Warburg效应:即使氧供充足,肿瘤细胞仍依赖有氧糖酵解(LDHA高表达),支持快速增殖。
谷氨酰胺成瘾:谷氨酰胺酶(GLS1)上调,维持TCA循环和核苷酸合成(靶向药物如CB-839在临床试验中)。
IDH突变与2-HG积累:2-HG竞争性抑制α-KG依赖性双加氧酶,导致组蛋白和DNA超甲基化,形成致瘤表观遗传景观。
6、肿瘤干细胞(GSCs)与治疗抵抗
GSCs标志物:CD133、Nestin、SOX2等,具有自我更新和分化潜能。
耐药机制:GSCs高表达ABC转运蛋白(如ABCG2)外排化疗药物;激活DNA损伤修复(如CHK1/2磷酸化)抵抗放疗;通过PD-L1表达或Treg浸润逃避免疫清除。
7、临床转化与靶向治疗
【分子分型指导治疗】
IDH突变型:IDH抑制剂(如Vorasidenib)联合表观遗传药物;
EGFR扩增型:EGFR靶向疗法(如西妥昔单抗)或抗体偶联药物(Depatuxizumab mafodotin)。
【免疫治疗突破】
CAR-T细胞靶向IL13Rα2或EGFRvIII;
PD-1抑制剂(纳武利尤单抗)联合放疗或抗血管生成药(贝伐珠单抗)。
【代谢靶向】
抑制IDH1突变(Ivosidenib)或谷氨酰胺代谢(Telaglenastat)。
脑癌的治疗需根据肿瘤类型、分级、分子特征、患者年龄及身体状况制定个体化方案,以 手术切除为基础,结合 放疗、化疗、靶向治疗及新兴疗法。
手术是多数脑癌的首选治疗,目标是 最大范围安全切除肿瘤(Maximal Safe Resection),同时保护神经功能。
1、手术方式
开颅肿瘤切除术:
神经导航与术中MRI:精确定位肿瘤边界,减少正常脑组织损伤。
术中唤醒麻醉:用于功能区(如语言区、运动区)肿瘤,实时监测神经功能。
立体定向活检:适用于深部或弥散性肿瘤(如脑干胶质瘤),明确病理诊断。
2、术后管理
并发症预防:控制脑水肿(地塞米松)、抗癫痫(左乙拉西坦)、预防深静脉血栓。
分子病理检测:检测IDH突变、1p/19q共缺失、MGMT启动子甲基化等,指导后续治疗。
放疗是脑癌(尤其高级别胶质瘤和转移瘤)的重要辅助治疗,分为传统外照射和新兴技术:
1、常规外照射
【适应症】
胶质母细胞瘤(GBM)术后标准治疗(Stupp方案:同步放化疗)。
转移性脑癌全脑放疗(WBRT)或立体定向放射外科(SRS)。
【剂量】
GBM:总剂量60 Gy,分30次(2 Gy/次)。
转移瘤SRS:单次15-24 Gy(限3-4个病灶)。
2、新兴技术
质子治疗:精准靶向肿瘤,减少周围脑组织损伤(适用于儿童和复发肿瘤)。
电场治疗(TTFields):通过低强度交变电场抑制肿瘤细胞分裂,联合替莫唑胺延长GBM生存期(中位OS 20.9个月)。
化疗在脑癌中的应用受限于 血脑屏障,需选择脂溶性或小分子药物:
1、常用药物及方案
替莫唑胺(TMZ):
适应症:GBM一线化疗(同步放疗+辅助治疗),MGMT甲基化者效果更佳。
用法:75 mg/m²(同步放化疗期间每日口服),后改为150-200 mg/m²(5天/28天周期)。
PCV方案(洛莫司汀+丙卡巴肼+长春新碱):用于少突胶质细胞瘤(1p/19q共缺失者)。
贝伐珠单抗(抗VEGF):控制脑水肿,用于复发GBM(单药或联合伊立替康)。
2、化疗敏感性差异
高敏感:少突胶质细胞瘤(1p/19q共缺失)、MGMT甲基化GBM。
低敏感:IDH野生型GBM、脑膜瘤。
1、靶向治疗
IDH抑制剂(如Ivosidenib):针对IDH1突变型低级别胶质瘤,延缓进展。
EGFR抑制剂(如厄洛替尼):用于EGFR扩增型GBM(疗效有限,常联合放疗)。
BRAF抑制剂(如达拉非尼+曲美替尼):治疗BRAF V600E突变型毛细胞星形细胞瘤或某些胶质瘤。
2、免疫治疗
PD-1/PD-L1抑制剂(如纳武利尤单抗):对高肿瘤突变负荷(TMB)或MSI-H脑癌可能有效,总体反应率低(<10%)。
CAR-T细胞疗法:靶向IL13Rα2或EGFRvIII的CAR-T在临床试验中显示潜力(如治疗复发性GBM).
1、单发转移
手术切除或 SRS(立体定向放射外科)联合全身治疗(如靶向药、免疫治疗)。
2、多发转移
全脑放疗(WBRT) 或 SRS联合免疫治疗(如肺癌脑转移用奥希替尼+放疗)。
脑水肿:地塞米松(起始剂量4-16 mg/天),逐渐减量防副作用(感染、高血糖)。
癫痫:左乙拉西坦(副作用少)、丙戊酸钠(避免与TMZ联用)。
静脉血栓:低分子肝素(如依诺肝素)抗凝,出血风险高时慎用。
抗体偶联药物(ADC):如Depatuxizumab(靶向EGFR),用于复发GBM。
溶瘤病毒:如G207(单纯疱疹病毒改造),诱导肿瘤免疫反应。
基因编辑:CRISPR技术敲除致癌基因(如TP53突变修复)。
本病可见于“头痛”、“眩晕”、“呕吐”、“中风”、“癫痫”等病中。
【辨证用方】
人体是一个有机的整体,脑病可及五脏,同样五脏病变也可及脑, 故诊治脑肿瘤可从脏论治。如脑与肝,脑肿瘤患者出现眩晕、痉厥、 头痛、癫狂等症状,通过凉肝熄风、平肝潜阳等,使肝魂得藏, 而脑神自安其宅;又如脑与脾,脑肿瘤患者出现头晕、神疲乏力、 气短懒言等症状,常通过补中益气、升理清阳,使脾意得安, 而脑神亦安;再如脑与肾,脑肿瘤患者出现髓海不足,见脑转耳鸣、 眩晕、健忘、腰酸等症状,常通过补肾填精,使肾精充而脑神安。
1、髓海不足
【主症】《灵枢·海论》云:“髓海不足,则脑转耳鸣,胫酸眩冒,目无所见, 懈怠安卧。”因肾主骨生髓,充于脑,若肾精不足,髓海亏乏,则出现目眩、 耳鸣、头低、神疲、不能久立、行走摇晃不稳等症状。
【治法】治宜填精补肾,肾精充,髓海得养,则脑髓自充,脑病自愈。
【主方】赵丽红治疗脑瘤验方
【组成与用法】蛇六谷30~60g, 天葵子30g, 生半夏15~30g, 生天南星15~30g, 夏枯草15g, 生牡蛎30g, 僵蚕12g, 生地黄、熟地黄各15g, 山茱萸10g, 枸杞子12g, 女贞子9g, 炙鳖甲9g, 炙龟板12g, 白蒺藜15g。水煎服。每日1剂, 早、晚分服。
【功能主治】滋补肝肾,化痰软坚。主治肝肾阴虚之脑瘤。
【加减应用】头痛明显者, 选加白芷6g, 川芎9g, 蔓荆子9g, 藁本9g; 呕吐明显者, 加姜半夏12g, 姜竹茹9g; 大便秘结者、选加枳实12g, 瓜蒌仁(打碎)30g,火麻仁(打碎)30g、生大黄(后下)9g; 肢体抽搐者,加全蝎3g,炙蜈蚣2条,天麻9g,钩藤12g; 视力障碍者,选加青稍子9g,密蒙花9g,石决明30g, 枸杞子12g,石斛夜光丸9g(分2次吞服)。
【方源】河南中医,2004,24(1):57-58.
2、上气不足
【主症】《灵枢·口问》云:“上气不足,脑为之不满,耳为之苦鸣, 头为之苦倾,目为之眩。”其中的上气即指脑之真气。上气不足即由 平日神机暗损,营血暗耗,以致脑气不足,脑失所养,而出现的耳鸣、 头倾、目眩、健忘、神疲、气怯,甚至肢体麻木等症状,严重者还可见晕厥。
【治法】治宜补养中气,升理清阳。
【主方】脑瘤平
【组成与用法】壁虎、蜈蚣、全蝎、水蛭各3g,薏苡仁、白花蛇舌草各30g, 黄芪15g,生晒参6g,姜半夏9g,川芎10g,白芷12g,白术15g,三棱9g, 补骨脂10g,枇杷叶、浙贝母各12g,酸枣仁15g,茯苓12g,甘草6g。 每日1剂,水煎服。
【功能主治】益气健脾,祛风化痰,祛瘀散结。主治脾肾气虚, 痰瘀交阻于脑之脑胶质瘤。
【方源】浙江中西医结合杂志,2021,31(7):675-67.
3、痰凝脑窍
【主症】脑为至清之腑,邪不能犯,犯之则病。若脏腑气机不畅, 体液循环受阻,导致痰浊内生,痰浊蒙蔽清窍,阻滞于脑腑或脑络, 神明受扰,则表现出面色暗滞、精神抑郁、神识迷蒙、急躁易怒、 哭笑无常、夜不入寐、饮食减少、舌苔厚腻、脉沉弦滑等症状。
【治法】治宜燥湿化痰,软坚散结。
【主方】息风软坚汤
【组成与用法】全蝎4.5g,蜈蚣6条,丹参20g,川芎4.5g,僵蚕9g, 地龙9g,半夏9g,钩藤15g,白术9g,天麻9g,天葵子15g,夏枯草30g, 川贝母9g,女贞子15g,枸杞子15g,松萝15g,分心木15g。水煎服。
【功能主治】息风清热,化瘀祛痰。主治脑瘤。
【加减应用】呕吐者加姜竹茹;头痛甚者加本、蔓荆子、白芷、菊花; 视力障碍者加蕤仁、青稍子、密蒙花、石决明、石斛夜光丸; 便秘者加大黄蛰虫丸或番泻叶;多饮多尿者加生地黄、天花粉、石斛、桑螵蛸、 龟板、远志。
【方源】浙江中医学院潘国贤方
4、瘀阻脑络
【主症】现代环境中的物理、化学性致癌因子及病毒等侵入人体, 影响气血流畅,阻滞脑络,引起头刺痛固定不移、健忘恍惚、半身不遂、 失语,或发狂、舌紫暗、舌面瘀斑、舌下络脉瘀阻、脉沉弦或弦涩等。
【治法】治宜活血化瘀,软坚散结,使脑络气血通畅,则脑瘤易消。
【主方】化痰散结法辨治脑瘤验方
【组成与用法】昆布20g,海藻20g,茯苓20g,莪术20g,壁虎2条,远志肉6g, 石菖蒲12g,生薏苡仁30g,陈皮20g,象贝母20g,夏枯草12g。每日1剂, 水煎服。
【功能主治】化痰,软坚,消肿。主治痰瘀互结之脑瘤。
【方源】江苏中医药,2015(8):49-50.
5、肝阳上亢
【主症】肝体阴而用阳,内藏魂,若精神情志失调,肝失疏泄,气郁日久化火, 肝阳偏亢,上扰清窍,又肝肾精血亏虚,水不涵木,阳气郁逆化风而上扰脑海, 占据清阳之位,则表现为头痛头晕、耳鸣目眩、心烦易怒、面红目赤、 失眠多梦、肢体麻木等。
【治法】治宜平肝潜阳,补益肝肾。
【主方】鱼脑石汤
【组成与用法】鱼脑石15g,广郁金12g,石菖蒲10g,天竺黄10g,石决明12g, 珍珠母24g,煅磁石3g,赤茯苓10g,橘络6g,橘红6g,地龙10g,桃仁10g, 钩藤12g,川牛膝25g,杭白芍12g,生赭石30g。水煎服。
【功能主治】化痰开窍,平肝潜阳。主治脑瘤。
【加减应用】虚火上炎者加生地黄、玄参;蒙心窍神魂恍惚及伏热呕吐者加服 安宫牛黄丸或局方至宝丹;肝阳上亢,眼目昏糊者加苦参、龙胆草、龙荟丸。
【方源】山东省肿瘤防治研究院史兰陵方
1、脑癌的总体生存率
总体生存率:根据美国癌症协会的数据,脑肿瘤患者的5年生存率约为36%,10年存活率接近31%。
年龄因素:生存率随年龄增长而下降。15岁以下人群的5年生存率超过74%,15-39岁人群的5年生存率约为71%,而40岁及以上人群的5年生存率约为21%。
2、不同类型脑癌的生存期
良性脑肿瘤:如脑膜瘤、听神经瘤等,通过手术完全切除后,患者通常可以获得长期生存,甚至不影响寿命。
恶性脑肿瘤
低级别胶质瘤(WHO Grade 2):5年生存率较高,可达60%以上,部分患者可存活10年甚至更久。
高级别胶质瘤(WHO Grade 3和4):如胶质母细胞瘤(GBM),中位生存期约为14.6-17个月,5年生存率不足10%。但随着新治疗方法的应用,部分患者可存活5年以上。
1、保持健康的生活规律
充足睡眠:保证每天8小时的睡眠,减少夜生活次数,降低脑肿瘤发病率。
规律作息:按时休息和睡眠,避免熬夜,保持规律的作息时间。
2、健康饮食
均衡饮食:摄入足够的水果、蔬菜和全谷类食品,富含维生素、矿物质和抗氧化剂,有助于提升身体免疫力。
避免刺激性食物:少吃辛辣、生冷、咸的食物,避免过量食用油腻、辛辣、腌制、熏烤等食物。
戒烟限酒:吸烟是脑癌的重要风险因素,戒烟可以降低患脑癌的风险。过量饮酒会增加患癌风险,建议限制酒精摄入,避免酗酒。
3、避免接触有害物质
避免电离辐射:减少长时间接触电离辐射源,如电视机、电脑、手机等。
避免有毒化学物质:避免长时间接触有毒有害的化学物质,如杀虫剂、苯并芘等。
4、定期体检
定期脑部检查:定期进行脑部检查,如CT或MRI等,及时发现疾病。
5、保持良好的心态
压力管理:学会调整心态和情绪,劳逸结合,避免过度劳累。
心情愉悦:保持心情愉悦和积极向上的生活态度,有助于提升身体免疫力。
6、加强体育锻炼
增强体质:适当的体育锻炼可以增强体质,提高免疫力,有助于预防脑癌。
晒太阳:在阳光下运动可以促进体内维生素D的合成,有助于骨骼健康和身体免疫力的提升。
1、基础护理
保持病室环境清洁:减少噪音和干扰,保持病室环境舒适。
定期评估生命体征:评估患者的生命体征、意识状态和肢体活动情况。
保持口腔、皮肤清洁:预防感染和压疮。
保证充足休息和睡眠:促进康复。
2、症状护理
头痛护理:采取适当的缓解措施,如遵医嘱使用药物、调整卧位等。
呕吐护理:保持患者口腔清洁,及时清理呕吐物,避免误吸和感染。
肢体功能障碍护理:进行被动肢体活动和功能训练,预防肌肉萎缩和关节僵硬。
语言障碍护理:进行语言康复训练,帮助患者恢复语言表达能力。
3、康复训练与指导
肢体功能康复:进行肢体肌力、关节活动度的训练,促进肢体功能恢复。
语言和认知功能康复:进行语言训练和认知功能训练,如语音疗法、记忆训练等。
心理康复:进行心理咨询和心理疏导,帮助患者调整心态,积极面对疾病。
4、营养与饮食
高蛋白、低脂肪、高纤维饮食:保证患者摄入足够的优质蛋白质,如鱼、肉、蛋、奶等。
维生素与矿物质补充:根据患者的具体情况,适当补充维生素和矿物质。
多样化饮食:提供多种食物,以满足患者全面的营养需求。
5、定期复查与随访
定期复查:治疗结束后应定期进行复查,以便及时发现复发或转移病灶。
随访管理:建立随访管理制度,对患者的病情状况、自身认知情况进行了解和评估,提供必要的指导和支持。
1、高蛋白摄入
2、补充充足的维生素和矿物质
3、适量的脂肪
4、少食多餐
5、选择易消化的食物
1、避免高脂肪类食物
2、避免高糖类食物
3、避免海鲜类食物
4、避免辛辣刺激性食物
5、避免油炸、腌制食物
6、避免咖啡等兴奋性饮料
7、避免酒精
食疗方 1
【组成】南瓜55克,虾皮20克,大白菜适量,面粉适量,葱姜、蒜、油各适量。
【制作】面粉加水调成硬度适中的面粉糊;将南瓜、大白菜虾皮、葱、姜、蒜一起剁碎制成馅,入一勺面糊摊成饼状,加一匙面糊摊匀,馅上再摊一层面粉糊,人油锅炸熟即可。
【功效】 适用于饮食不振、浮肿、少尿的癌症病人。
备注:更多食疗方见肿瘤药膳专栏,或点击本页相关文章栏目相应文章链接阅读。